سفارش ترجمه متون تخصصی ترمودینامیک
ترجمه تخصصی مقالات، گزارشات، متون علمی و کتب علمی - دانشگاهی در موضوع ترمودینامیک توسط سایت ما ارائه و پشتیبانی می شوند.
جهت سفارش ترجمه با سرپرست تیم مترجم سایت ما تماس بگیرید.
سرپرست تیم ترجمه: مهندس محمد علایی
ایمیل: Translate@Tnt3.ir
تلفن همراه: 09192164907
Telegram: @ChiefTranslator
ترمودینامیک (به یونانی: θερμο «گرما» + δυναμική «توان و قدرت») و (به فرانسوی: Thermodynamique)، شاخهای از علوم طبیعی است که به بحث راجع به گرما و نسبت آن با انرژی و کار میپردازد. ترمودینامیک متغیرهای ماکروسکوپیک (همانند دما، انرژی داخلی، آنتروپی و فشار) را برای توصیف حالت مواد تعریف و چگونگی ارتباط آنها و قوانین حاکم بر آنها را بیان مینماید. ترمودینامیک رفتار میانگینی از تعداد زیادی از ذرات میکروسکوپیک را بیان میکند. فوانین حاکم بر ترمودینامیک را از طریق مکانیک آماری نیز میتوان بدست آورد.
ترمودینامیک موضوع بخش گستردهای از علم و مهندسی است - همانند: موتور، گذار فاز، واکنشهای شیمیایی، پدیدههای انتقال و حتی سیاه چاله ها-. محاسبات ترمودینامیکی برای زمینههای فیزیک، شیمی، مهندسی نفت، مهندسی شیمی، مهندسی هوافضا، مهندسی مکانیک، زیستشناسی یاخته، مهندسی پزشکی، دانش مواد و حتی اقتصاد لازم است.
عمده بحثهای تجربی ترمودینامیک در چهار قانون بنیادی آن بیان گردیدهاند: قانون صفرم، اول، دوم و سوم ترمودینامیک. قانون اول وجود خاصیتی از سیستم ترمودینامیکی به نام انرژی داخلی را بیان میکند. این انرژی از انرژی جنبشی که ناشی از حرکت کلی سیستم و انرژی پتانسیل که سیستم نسبت به محیط پیرامونش دارد، متمایز است. قانون اول همچنین دو شیوه انتقال انرژی یک سیستم بسته را بیان میکند: انجام کار یا انتقال حرارت. قانون دوم به دو خاصیت سیستم، دما و آنتروپی، مربوط است. آنتروپی محدودیتها - ناشی از برگشتناپذیری سیستم - بر میزان کار ترمودینامیکی قابل تحویل به یک سیستم بیرونی طی یک فرایند ترمودینامیکی را بیان میکند. دما، خاصیتی که با قانون صفرم ترمودینامیک تا حدودی تبیین میگردد، نشان دهندهٔ جهت انتقال انرژی حرارتی (گرما) بین دو سیستم در نزدیکی یکدیگر است. این خاصیت همچنین به صورت کیفی با واژههای داغ یا سرد بیان میگردد.
از دیدگاه تاریخی ترمودینامیک با آرزوی افزایش بازده موتورهای بخار گسترش یافت. به ویژه به سبب تلاشهای فیزیکدان فرانسوی، نیکولا لئونارد سعدی کارنو که اعتقاد داشت افزایش بازده موتورهای بخار میتواند رمز پیروزی فرانسه در نبردها ناپلئون باشد. فیزیکدان انگلیسی، لرد کلوین، نخستین کسی بود که در سال ۱۸۵۴ تعریفی کوتاه برای ترمودینامیک ارائه داد:
در ابتدا ترمودینامیک ماشینهای بخار به صورت عمده راجع به خصوصیات گرمایی مواد مورد کاربرد- بخار آب - بود. بعدها این مبحث به فرایندهای انتقال انرژی در واکنشهای شیمیایی مرتبط گردید. ترمودینامیک شیمیایی اثر آنتروپی بر فرایندهای شیمیایی را مورد بحث قرار میدهد. همچنین ترمودینامیک آماری (یا مکانیک آماری) با پیش بینیهای آماری از رفتار ذرات سیستم، ترمودینامیک ماکروسکوپیک را توجیه مینماید.
ترمودینامیک (ریشهٔ یونانی دارد و از دو بخش θερμη به معنی گرما و δυναμις به معنی نیرو تشکیل شده که سرهم بندی این دو کلمه٬ نیروی گرما بوجود میآید[۱]) شاخهای از فیزیک و شیمی است که پدیدههای ماکروسکوپیک که از تغییر دما، فشار و حجم در یک سیستم فیزیکی اتفاق میافتد بررسی میکند.[۲][۳]
شروع ترمودینامیک از ساخت اولین پمپ خلأ در سال ۱۶۵۰ میلادی و توسط اتو وان گریکه شروع شد اتو ثابت کرد که نظریه ارسطو مبنی بر اینکه طبیعت از خلا متنفر است، اشتباه است. مدتی بعد فیزیکدان و شیمیدان ایرلندی رابرت بویل طرز کار دستگاه جریکو را یاد گرفت و به همراه فیزیکدان انگلیسی رابرت هوک توانست اولین پمپ هوا را در سال ۱۶۵۶ بسازد.[۴] و بین حجم و فشار رابطهای تعریف کردند، که امروزه به قانون بویل مشهور است. سپس در سال ۱۶۷۹ شریک بویل دنیس پاپین اولین steam digester را ساخت که یک ظرف دربسته با در محکم بود که در آن بخار با فشار بالا تولید میشد.
مفاهیم پایه برای گرمای ویژه و گرمای ویژه نهان توسط جوزف بلک در دانشگاه گلاسکو، جایی که جیمز وات به عنوان ابزار ساز کار میکرد آرایه شد. جیمز وات با بلک در باره افزایش بازدهی موتور بخار مشورت کرد اما این خود وات بود که ضرورت وجود چگالنده بخار خارجی را برای افزایش بازدهی گرمایی موتور بخار پیشبینی نمود. سعدی کارنو، پدر ترمودینامیک، با توجه به تمامی کارهای قبلی مقالهای با عنوان ایدههایی در باره حرکت جنبشی آتش منتشر نمود. این مقاله در باره گرما٬ قدرت٬ انرژی٬ و بازدهی موتور بحث میکرد. این مقاله روابط بین موتور کارنو٬ چرخه کارنو٬ و قدرت حرکتی را مورد بحث قرار میداد. مقاله کارنو سرآغازی بر علم ترمودینامیک به عنوان دانشی نوین شد.
نخستین کتاب ترمودینامیک توسط ویلیام رانکین٬ که فیزیک خوانده بود و به عنوان استاد مهندسی مکانیک و عمران در دانشگاه گلاسکو کار میکرد٬ در سال ۱۸۵۹ منتشر گردید. همزمان قانون اول و قانون دوم ترمودینامیک در دهه ۱۸۵۰ میلادی بر اساس کارهای رانکین، رودلف کلاوزیوس و ویلیام تامسون نگاشته شد.
مبانی ترمودینامیک آماری توسط جیمز کلرک ماکسول، لودویگ بولتزمان، ماکس پلانک، رودلف کلاوزیوس و جوسایا ویلارد گیبس بنیان گذاشته شد. در بین سالهای ۱۸۷۳ تا ۱۸۷۶ جوسایا ویلارد گیبس سه مقاله منتشر نمود که مشهور ترین آنها تعادل مواد ناهمگون میباشد. گیبس همچنین نشان داد که چگونه پروسههای ترمودینامیکی شامل فعل و انفعالات شیمیایی را میتوان بصورت نموداری نشان داد، او نشان داد که چگونه میتوان روی دادن خود به خودی واکنشها را از روی انرژی، انتروپی، حجم، پتانسیل شیمیایی، دما و فشار در سیستمهای ترمودینامیکی پیشبینی نمود. ترمودینامیک شیمیایی بعد تر توسط پیر دوهام، گیلبرت لوویس، مرل لاندل و ادوارد گوگنهایم توسعه بیشتر یافت.
علم ترمودینامیک به بررسی سیستمهای فیزیکی بر اساس تئوریها و قوانین ترمودینامیک میپردازد. بسته به مبانی اولیه به کار رفته علم ترمودینامیک به شاخههای مختلف تقسیم شده است.
مبنای ترمودینامیک کلاسیک برا اساس تبادل انرژی در فرایندی در درون چرخه میباشد، تبادل انرژی مابین سیستمهای بسته تنها با در نظر گرفتن تعادل ترمودینامیکی آنها میباشد. همچنین شناسایی کار و گرما به عنوان انرژی در ترمودینامیک کلاسیک ضروری میباشد.
ترمودینامیک آماری، یا مکانیک آماری، در نیمه دوم قرن نوزدهم و نیمه اول قرن بیستم با پیشرفت و شناسایی تئوریهای مولکولی و اتمی بنیان نهاده شد. این علم توضیحات و ادله برای قوانین ترمودینامیک کلاسیک بیان میکند. ترمودینامیک آماری واکنشهای بین مولکولی و همچنین حرکت دسته جمعی مولکولها بیان میکند.
یکی از مفاهیم اصلی در ترمودینامیک سیستم میباشد. سیستم ناحیهای از فضا است که برای بررسی انتخاب میشود. به هر آنچه که خارج از این سیستم وجود دارد محیط گفته میشود. سیستم بوسیله مرزی از محیط جدا میشود. این مرز میتواند مرزی واقعی یا مجازی باشد. سیستم میتواند از طریق این مرز انرژی و جرم با مبادله نماید. پس به طور خلاصه داریم:
بدون تبادل ماده
بدون تبادل ماده
برای توصیف هر فرایند، باید حاتهای ابتدایی و انتهایی فرایند، مسیر فرایند و برهمنکنشها را با اطراف مشخص کنیم. فرایندها به دو نوع عمده برگشتپذیر و برگشتناپذیر تقسیم میشوند.
دستهبندی دیگر فرایندها بصورت زیر است:
قانون صفرم ترمودینامیک بیان میکند که اگر دو سیستم با سیستم سومی در حال تعادل گرمایی باشند، با یکدیگر همدما میباشند. به طور مثال اگر جسم a باجسم b درتعال گرمایی باشد وجسم b باجسم c درتعادل گرمایی باشد میتوان گفت جسم a و c در تعادل گرمایی میباشد. اساس ساخت دمانسج قانون صفرم ترمودینامیک میباشد به این صورت که هوای محیط باشیشهٔ دماسنج در تعادل حرارتی است وشیشه دماسنج نیز با جیوه در تعادل حرارتی است در نتیجه طبق قانون صفرم ترمودینامیک هوا با جیوه نیز در تعادل میباشد.
انرژی درونی یک سیستم منزوی ثابت و پایدار است. قانون اول ترمودینامیک که به عنوان قانون بقای کار و انرژی نیز شناخته میشود، میگوید: تغییر انرژی درونی یک سیستم برابر است با مجموع گرمای داده شده به سیستم و کار انجام شده بر آن:
ساخت یک موتور سیکلی که تأثیری جز انتقال مداوم گرما از دمای سرد به دمای گرم نداشته باشد، غیر ممکن است. بیان کلوین-پلانک: غیرممکن است وسیلهای بسازیم که در یک سیکل عمل کند و در عین حال فقط با یک مخزن تبادل حرارت داشته باشد یعنی غیر ممکن است یک موتور حرارتی بدون از دست دادن گرمادر Qc به کار خود ادامه دهد. بیان کلازیوس:امکان ندارد که یک یخچال طی یک چرخه، تمام انرژی را که از منبع سرد دریافت میکند به منبع گرم انتقال دهد. یعنی نمیتوان یخچالی ساخت که بدون کار ورودی عمل کند. به عبارت ساده قانون دوم بیانگر مسیر انجام یک فرایند میباشد.
قانون سوم ترمودینامیک میگوید هنگامی که انرژی یک سیستم به حداقل مقدار خود میل میکند، انتروپی System به مقدار قابل چشمپوشی میرسد. یا بطور نمادین: هنگامی که  ،
، 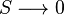
پتانسیلهای ترمودینامیکی، متغیرهای اسکالری میباشند که برای ارزیابی انرژی ذخیره شده در سیستم استفاده میشوند. پتانسیلها برای اندازهگیری تغییرات انرژی هنگامی که از حالت اولیه به حالت نهایی استفاده میشوند. از پتانسیلهای مختلف با توجه به متقییرهای محدود کننده در سیستم همانند فشار و حجم استفاده مشود. به عنوان مثال هر دو پتانسیل گیبز و هلمهولتز به عنوان انرژی قابل دسترس برای انجام کار مفید شناخته میشوند هنگامی که به ترتیب فشار و دما یا حجم و دما در سیستم ثابت نگه داشته شوند. پنج پتانسیل مهم در ترمودینامیک بصورت جدول زیر تعریف شدهاند:
در جدول فوق  فشار،
فشار، 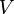 حجم،
حجم،  دما و
دما و 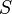 آنتروپی میباشد. روابط ماکسول با توجه به این چهار پتانسیل تعریف میشوند.
آنتروپی میباشد. روابط ماکسول با توجه به این چهار پتانسیل تعریف میشوند.
